El cáncer es una enfermedad asociada a la edad y al envejecimiento, ya que se da más frecuentemente en personas de edad avanzada. Aun así, un estudio publicado en The Lancet dio a conocer que alrededor de 400.000 niños y adolescentes (de 0 a 19 años) son diagnosticados con cáncer anualmente [1]. Entonces, ¿por qué aparece el cáncer en pacientes jóvenes de forma ocasional?
Lamentablemente, no hay aun una respuesta clara a esta pregunta, ya que: los efectos perjudiciales asociados a un estilo de vida no saludable aún no han tenido tiempo de manifestarse; la acumulación de mutaciones genéticas asociada a la edad aún no ha sucedido; y hay evidencias de que tan sólo un pequeño porcentaje de cánceres infantiles (~10%) tienen una causa genética directa [2]. Las grandes mejoras en el tratamiento del cáncer infantil han incrementado la supervivencia general de estos pacientes, que ha pasado de un 20-30% (en los años 1960) a un 80-85% a día de hoy. Estos avances han sido posible sobre todo al descubrimiento de las mejores combinaciones de fármacos quimioterapéuticos para cada tipo de cáncer infantil, así como la optimización de las dosis de cada uno.
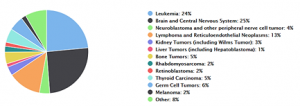
Sin embargo, no todo es tan bonito como suena: hay un subconjunto de niños y niñas con cáncer muy avanzado, metástasis o con tipos de cáncer particularmente malignos, en los que la supervivencia no supera el 30%. Por algún motivo, estos tipos de tumores son resistentes al tratamiento, es decir que las células cancerígenas tienen la capacidad de sobrevivir a los fármacos y seguir proliferando. Es más, estos tratamientos a menudo causan efectos secundarios que pueden ser graves o incluso letales. Nunca antes se ha conseguido aumentar la supervivencia en este grupo de pacientes de mal pronóstico. De hecho, la supervivencia general de todos los pacientes de cáncer infantil se ha estancado en las últimas décadas sobre el 80-85%. Este dato parece indicar que ya hemos exprimido el máximo potencial de los fármacos quimioterapéuticos, y es probable que cualquier combinación de este tipo de fármacos no sobrepase la eficacia de otras terapias ya existentes para el cáncer infantil. Por ello, es crucial descubrir nuevas medicinas que mejoren la gestión clínica de estos jóvenes pacientes.
Las llamadas “terapias moleculares dirigidas” han revolucionado el campo de la farmacología y el descubrimiento de fármacos en el cáncer. Normalmente, la quimioterapia consiste en la administración de compuestos químicos tóxicos que actúan por todo el cuerpo, atacando predominantemente a las células que se dividen rápidamente (como son las células cancerosas). No obstante, la quimioterapia da lugar a efectos secundarios ya que hay una parte de células sanas que también sufren daños debido al amplio rango de acción de estos fármacos. Por el contrario, las terapias moleculares dirigidas son agentes biológicos o compuestos que bloquean o interfieren con las “dianas terapéuticas”, que no son más que componentes celulares específicos (p.ej., moléculas, proteínas, vías de señalización, etc.) de las células cancerosas y que, de alguna forma, están involucradas en el crecimiento y la diseminación del cáncer [4]. De esta forma, las terapias dirigidas tienen ventajas clave con respecto a la quimioterapia: tienen una acción más selectiva contra las células tumorales (la eficacia es mayor) y los efectos secundarios son menores. Por ello, se las considera como la mejor solución para acrecentar las estadísticas de supervivencia en estos jóvenes pacientes con tumores agresivos.
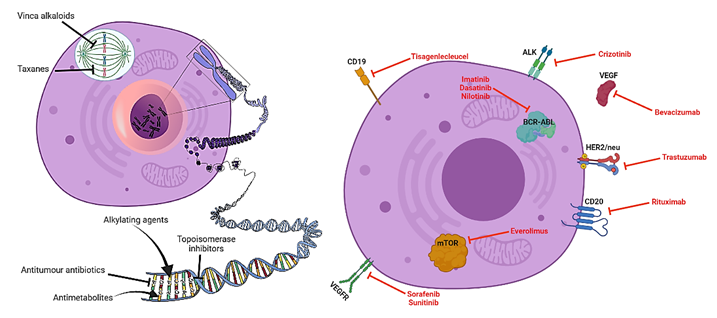
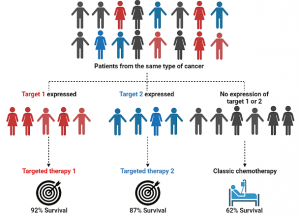
El hallazgo de las terapias dirigidas surge del creciente conocimiento sobre las características moleculares y biológicas de los tumores. Las nuevas técnicas moleculares permiten cosechar grandes cantidades de datos biológicos sobre los tumores y descubrir potenciales dianas a una velocidad sin precedentes. Además, hoy podemos diferenciar diferentes subtipos de un mismo tipo de cáncer en función de diferentes propiedades moleculares. Esta ramificación de los pacientes con cáncer significa que ahora no solo le podemos poner nombre a un cáncer, sino que también le podemos dar un apellido. Consecuentemente, los tumores con el mismo nombre, pero distinto apellido, pueden tratarse de forma diferente con terapias dirigidas. Éste es el principio fundamental de la medicina personalizada o medicina de precisión. Un ejemplo muy representativo es el del cáncer de mama (nombre). Es el tipo de cáncer más común en mujeres, y se puede clasificar en varios subtipos (apellido) dependiendo de las características biológicas, como HER2+, ER+, BRCA+, Triple Negativo, etc. [5]. Varias terapias moleculares están disponibles para tratar cada uno de estos subtipos, lo cual ha contribuido a incrementar radicalmente la supervivencia de las pacientes de cáncer de mama hasta un 90% [6].
En mi doctorado, estoy centrado en el estudio de un tipo de cáncer infantil conocido como Rabdomiosarcoma. Actualmente es uno de los cánceres infantiles más mortíferos, y se origina esencialmente en el músculo esquelético (músculos bajo control voluntario, responsables de nuestro movimiento físico), aunque su origen real no se sabe con certeza. En nuestro laboratorio estamos intentando desarrollar un tipo de terapia dirigida para esta enfermedad, usando las enzimas CYP450 como dianas. Los CYP450 son un grupo muy extenso de enzimas en nuestro organismo que llevan a cabo muchas reacciones químicas y metabólicas, incluyendo el metabolismo de fármacos. Algunos estudios sugieren que hay ciertas clases de enzimas CYP450 se encuentran únicamente expresadas en los tumores de Rabdomiosarcoma7. El hecho de que la diana se encuentre solo en el tejido tumoral es clave, ya que queremos aprovechar la capacidad de estas enzimas de activar profármacos. Los profármacos son, en pocas palabras, fármacos en una forma inactiva que pasan a activarse en un fármaco funcional cuando son metabolizados por ciertas enzimas. Desde luego, si las enzimas diana se encuentran expresadas en otros tejidos sanos, el profármaco se activará en otras áreas del cuerpo fuera del tumor, causando efectos secundarios. Para intentar evitarlo, hemos diseñado profármacos que son activados específicamente cuando son metabolizados por las enzimas CYP450 presentes en las células de Rabdomiosarcoma. Por lo tanto, nuestra hipótesis es que estos profármacos, activados por enzimas CYP450, podrían constituir un tratamiento ideal para el Rabdomiosarcoma, dado que la forma activa del fármaco se liberaría de forma muy selectiva en el tumor, teniendo un efecto mucho más localizado y reduciendo la posibilidad de causar efectos secundarios.
Tabla 1.Lista de terapias moleculares dirigidas actualmente aprobadas para el tratamiento de cánceres infantiles. El nombre del fármaco (izquierda), indicaciones para cáncer infantil (centro) y el nombre de la diana molecular a la que inhiben (derecha) están indicados.
| Fármaco | Indicaciones | Diana |
| Denosumab | Cáncer de Hueso | RANKL |
| Ipilimumab | Cáncer Colorrectal, Melanoma | CTLA-4 |
| Nivolumab | Cáncer Colorrectal | PD-1 |
| Everolimus | Astrocitoma de Células Gigantes | m-TOR |
| Pembrolizumab | Linfoma de Hodgkin, Linfoma de Non-Hodgkin, Carcinoma de Células de Merkel | PD-1 |
| Blinatumomab | Leucemia Linfoblástica Aguda | CD19 / CD3 |
| Dasatinib | Leucemia Linfoblástica Aguda, Leucemia Mieloide Crónica | BCR-ABL |
| Imatinib | Leucemia Linfoblástica Aguda, Leucemia Mieloide Crónica | BCR-ABL |
| Tisagenlecleucel | Leucemia Linfoblástica Aguda | CD19 |
| Gemtuzumab Ozogamicin | Leucemia Mieloide Aguda | CD33 |
| Tagraxofusp | Neoplasia Blástica de Células Dendríticas Plasmacitoides | CD123 |
| Nilotinib | Leucemia Mieloide Crónica | BCR-ABL |
| Avelumab | Carcinoma de Células de Merkel | PD-L1 |
| Dinutuximab | Neuroblastoma | GD2 |
| Naxitamab | Neuroblastoma | GD2 |
| Selumetinib | Neurofibromatosis de Tipo I | MEK1/2 |
| Crizotinib | Linfoma de Non-Hodgkin, Linfoma Anaplásico de Células Grande | ALK |
| Entrectinib | Varios tumores sólidos | TrkA/B/C, ALK, ROS1 |
| Larotrectinib sulfate | Varios tumores sólidos | Trk |
A pesar de ser bastante recientes, la incursión de las terapias moleculares dirigidas en el panorama del tratamiento del cáncer ya ha proporcionado efectos extraordinariamente positivos en adultos. Aunque algunas de estas terapias ya se usan a día de hoy para tratar a niños con cáncer (Tabla 1), históricamente la legislación siempre ha puesto palos en las ruedas para su evaluación y aprobación en estos pacientes. Por este motivo, el tratamiento de niños con cáncer siempre ha estado algo atrasado en comparación con el tratamiento de cáncer en adultos. Recientemente, los órganos reguladores del sector están tomando consciencia de este problema, y están empezando a revertir esta serie de políticas para apoyar el desarrollo de más terapias dirigidas para el cáncer infantil. Si nosotros, como comunidad científica, somos capaces de fomentar el desarrollo de estas terapias para el cáncer infantil durante los próximos años, las tasas de supervivencia van a aumentar indudablemente en estos pequeños héroes. ¡Hagámoslo realidad!
Por Enric Arasanz Picher (@EnricArasanz), estudiante de doctorado en la Universidad de Bradford.
Más información: