El oxígeno es algo tan común como respirar — ¡ y nunca mejor dicho! Sin embargo, no es tan simple como podamos pensar. Cuando hablamos de oxígeno, nos referimos también al tercer elemento más abundante del universo en cuanto a su masa, justo detrás del hidrógeno y del helio.
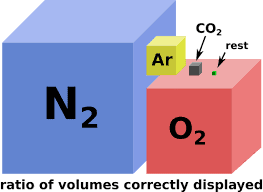
Los óxidos, unos compuestos formados por al menos un átomo de oxígeno y algún otro elemento, constituyen casi la mitad de la corteza terrestre [1]. Bajo presión y temperatura estándar, los átomos de oxígeno se unen de dos en dos para formar una molécula de oxígeno diatómico. Como seguramente hayas leído en alguna ocasión, el resultado lleva a la famosa fórmula del oxígeno: O2. Aunque el nitrógeno, con un 78% aproximadamente, domina la composición de la atmósfera del planeta en nuestros días, hay que recordar que el oxígeno diatómico constituye aproximadamente un 21% de la atmósfera terrestre actual. A su vez, dicha composición se completa con pequeñas cantidades de argón, dióxido de carbono y vapor de agua. Aunque todo lo que has leído hasta ahora puede sonar muy común, en verdad no siempre ha sido así.
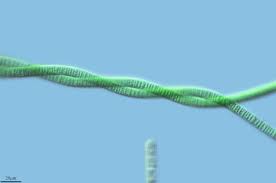
Se cree que la atmósfera previa a la aparición de los seres vivos era fuertemente reductora, es decir, carente de oxígeno en estado libre. Su composición estaba dominada por nitrógeno, dióxido de carbono y metano, un ambiente totalmente irrespirable para nosotros. No fue hasta hace unos 2.500 millones de años que no se alcanzaron concentraciones apreciables de oxígeno [2]. La presencia de grandes cantidades de oxígeno disuelto y en estado libre pudo llevar a la extinción a la mayoría de organismos que existían por aquel entonces. El metabolismo de estos seres no dependía del oxígeno, por lo cual se les conoce como anaerobios. De hecho, el oxígeno es un potente tóxico para ellos. Esta subida en los niveles de oxígeno se atribuye a la fotosíntesis de las cianobacterias, organismos que se cree que se desarrollaron hace unos 3.500 millones de años. El oxígeno en estado libre proviene de la ruptura del agua durante la fotosíntesis mediada por la luz. Se estima que las algas verdes y las cianobacterias de los mares y océanos producen un 70% del total de oxígeno siendo producto de las plantas terrestres el 30% restante [3]. De este modo, y sin quitarle la importancia que obviamente tiene, tal vez habría que replantearse la denominación de la selva amazónica como “el pulmón del planeta” en favor de los océanos.
La reacción general de la fotosíntesis (6 CO2 + 6 H2O + fotones → C6H12O6 + 6 O2) nos indica que los organismos fotosintéticos consiguen sintetizar azúcares (C6H12O6) a partir de dióxido de carbono (CO2) agua (H2O) empleando en este proceso la energía luminosa (i.e., fotones) en este proceso. El oxígeno en esta fórmula (O2) es un «producto de deshecho» que se genera a partir de este proceso y, como tal, se libera por estos organismos a la atmósfera. Y aquí empieza lo bueno.

La presencia de oxígeno en la atmósfera posibilitó el desarrollo de la respiración aerobia, la cual dependen del O2 y se encuentra presente en todos los eucariotas (por lo tanto, también en los organismos multicelulares superiores como las plantas y los animales). Esta estrategia metabólica produce una cantidad de energía mucho mayor que la de los organismos anaerobios e hizo posible que se generaran formas de vida más complejas y, por lo tanto, de mayor demanda energética. Otra importante función del oxígeno se consigue cuando forma un trío, esto es, cuando tres átomos de oxígeno se unen en una molécula. En dicho caso, se genera ozono (O3), compuesto que conforma una capa en la troposfera y que nos protege de la radiación ultravioleta procedente del sol y que, de otra manera, alcanzaría la superficie terrestre y dañaría los seres vivos. Éste es el ozono “bueno”. No obstante, también existe el ozono “malo”, aquél que está “dónde no debe”: en la superficie terrestre (o troposfera). En este caso, el ozono se convierte en un agente perjudicial para los seres vivos ya que causa numerosos problemas respiratorios.
La presencia de oxígeno en la atmósfera también hizo posible la aparición de unas moléculas denominadas especies reactivas del oxígeno (EROS, también conocidas por sus siglas inglesas ROS, reactive oxygen species). La más conocida de estas moléculas es la famosa agua oxigenada (H2O2). Las EROS son moléculas que están presentes de forma natural en bajas concentraciones en células de todo tipo, donde desempeñan diversos papeles fisiológicos tales como la señalización celular, la homeostasis y la defensa frente a organismos invasores. Sin embargo, bajo determinadas circunstancias, los niveles de las EROS pueden aumentar más allá de los niveles fisiológicos y, dado su elevada capacidad reactiva, pueden causar daños en todo tipo de biomoléculas, lo que se denomina «estrés oxidativo». De este modo, las EROS desempeñan un papel dual; si actúan de modo fisiológico o como elementos dañinos depende del balance entre su producción y su eliminación [4,5]. En otras palabras, la toxicidad del oxígeno puede devenir tanto de una producción descontrolada de EROS como de una ineficiente eliminación de las mismas por parte del sistema antioxidante.
Tal y como vemos, el oxígeno es un elemento de gran potencia y valor. No es de extrañar, por lo tanto, que los seres aerobios dispongamos de un sistema sensor de los niveles de oxígeno en nuestro organismo, tema que será la base de mi próximo post en el Blog CERU — ¡estad atentos!
Como último apunte, recordemos que un humano adulto en reposo inhala unos 2 gramos de oxígeno por minuto [6]. Esto implica que, anualmente, la humanidad consume más de 6.000 millones de toneladas de oxígeno que, como hemos dicho, proviene de la naturaleza, los seres fotosintéticos, las plantas. Por tanto, cabe reflexionar que dadas las circunstancias que vivimos respecto a la salud de nuestro planeta, debemos esperar y desear que los seres fotosintéticos sigan siendo capaces de producir toda esta cantidad de oxígeno, un elemento vital para todos los seres vivos.
Por Jose María Cabeza Fernández. Técnico especialista en el Instituto de Biomedicina en Sevilla (IBiS).
Más información:
- Atkins P et al. (2016). Chemical Principles, 7th edition. Freeman. ISBN 978-1-4641-8395-9.
- Informacióna vía Wikipedia sobre la Paleoatmósfera, disponible online aquí.
- Fenical, W (983). Marine Plants: A Unique and Unexplored Resource. Plants: the potentials for extracting protein, medicines, and other useful chemicals (workshop proceedings). DianePublishing. p. 147. ISBN 978-1-4289-2397-3. Disponible online aquí.
- Waszczak, et al. (2018).
- Edreva, A (2005).
- Flow restrictor for measuring respiratory parameters, patente US622456-B1, búsqueda llevada en google aquí.