¿Cuántas veces hemos escuchado que la naturaleza es sabia y que podemos aprender mucho de ella? Cientos, ¿verdad? Pues bien, en esta entrada os traigo otro ejemplo de ello, ¡pero con novedades!
La luz solar nos aporta energía que podemos aprovechar en forma de calor o electricidad mediante paneles solares térmicos o fotovoltaicos, entre otros. Vale, esto ya lo conocemos todos. Sin embargo, ¿y si os dijera que esa misma luz solar puede, además, eliminar el CO2 de, por ejemplo, la corriente de gases de una industria? Esto suena ya más novedoso, ¿verdad? O quizás no porque, si pensamos bien, las plantas hacen algo similar durante el proceso de fotosíntesis: convierten el agua y el CO2 presente en el aire en azúcares, alcoholes y oxígeno gracias a la luz del sol. De forma similar a la fotosíntesis, existen equipos que, además de generar energía almacenable en forma de combustible, son capaces de captar el CO2.
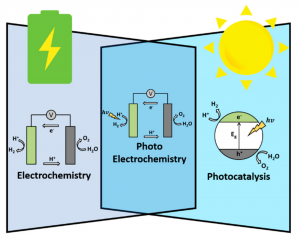
La fotoelectroquímica resume los tres conceptos que hacen funcionar a estos equipos llamados celdas fotoelectroquímicas. Los fotones (luz solar) activan y son capaces de aportar la energía necesaria para mover los electrones de determinados compuestos (CO2, H2O, etc.) presentes en las celdas, de forma que consiguen combinar unos (CO2) con otros (H2O) formando nuevos compuestos químicos como, por ejemplo, metano (CH4); que es el principal componente del gas natural (sí, ese gas que nos llega a casa). En otras palabras, los fotones de la luz solar ayudan a que se produzcan reacciones químicas de determinados compuestos (también conocidos como reactivos) para generar nuevos productos. Este proceso se lleva a cabo gracias al transporte de electrones entre reactivos y productos y con la mediación de otros compuestos llamados electrocatalizadores. Esto quiere decir que, si escoges adecuadamente los reactivos, puedes obtener el producto que te interese. Consecuentemente, una de las aplicaciones de los sistemas fotoelectroquímicos es la conversión del CO2 en combustibles y productos químicos de valor en la industria. Algunos autores denominan a este proceso fotosíntesis artificial, conocido también como producción de combustibles de carbono solares.
En el contexto energético y ambiental en el que nos encontramos actualmente, uno de los grandes retos de nuestra sociedad es aunar el uso de energías provenientes de fuentes renovables, como el sol, con la gestión de la actual demanda energética. La generación de energía con energías renovables se caracteriza por una alta intermitencia y variabilidad. Esto supone que se necesita disponer de un adecuado almacenamiento de la energía generada para así poder hacer uso de ella a posteriori cuando nos interese. Además, todo ello debe realizarse con una gestión medioambientalmente sostenible, es decir, que todo este proceso se haga sin contaminar ni aumentar las emisiones netas de CO2.
Los sistemas para la conversión solar del CO2 en combustibles y compuestos químicos se pueden dividir en tres grupos: sistemas fotocatalíticos (PC), sistemas electroquímicos alimentados por celdas fotovoltaicas (PV-EC) y sistemas fotoelectroquímicos (PEC). A continuación, os hablaré de este último.
Los sistemas PEC constan, fundamentalmente, de dos electrodos: un electrolito y el electrocatalizador. En algunos casos, también presentan una membrana de separación entre las cámaras anódica y catódica. Uno de los electrodos (a veces incluso ambos) están hechos de un material semiconductor fotoactivo (fotoelectrodo) y se llaman fotoánodo y fotocátodo, dependiendo de cuál reciba la luz solar. También hay celdas en las que ambos electrodos pueden estar iluminados. En las siguientes figuras se muestran los esquemas de configuraciones de celdas fotoelectroquímicas de tres electrodos.
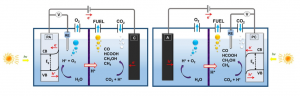
El modelo que simula lo que sucede dentro de la celda considera que en el ánodo se produce la reacción de oxidación del agua. En esta reacción, el CO2 se reduce a compuestos orgánicos como el metano en el cátodo. Para ello, los protones (H+) atraviesan la membrana que separan las dos semiceldas. Las reacciones redox (término usado para describir reacciones de oxidación y reducción) son:
Semirreacción ánodo: 2H2O –> O2 + 4e– + 4H+ ; E0 = -1.23 V (E0 vs. NHE a pH=0)
Semirreacción cátodo: CO2 + 8H+ + 8e– –> CH4 + 2H2O; E0 = 0.17 V (E0 vs. NHE a pH=0)
Estos sistemas no son termodinámicamente favorables, es decir, necesitan un aporte externo de energía para favorecer el movimiento de los electrones y que se produzcan las reacciones en cada electrodo; esto se realiza aplicando un potencial eléctrico (V). Hay que tener en cuenta que la energía necesaria depende de la cantidad de electrones a “movilizar” en la reacción y de lo estable que sea la molécula. Por ejemplo, el CO2 es un compuesto muy estable y, por tanto, algo más costoso (energéticamente hablando) que el hidrógeno. Por ello, estos sistemas de producción de “combustibles solares” solo tienen sentido si se enfocan como almacenamiento de electricidad producida por energías renovables excedentes. Esta electricidad renovable sería la que alimentaría la celda fotoelectroquímica y ésta convertiría el CO2 en combustibles como el metano, componente principal del gas natural.
En caso de que se quiera obtener el metano como combustible solar almacenable, recientes publicaciones reportan eficiencias faradaicas del 67% [2], lo que supone una tasa de conversión de CO2 a CH4 superior al 80%. Eso sí, éste no es el único compuesto de base carbonosa que se puede obtener. Otros productos de gran valor en la industria son el ácido fórmico, metanol, etanol y monóxido de carbono [1]. Para caracterizar adecuadamente el funcionamiento de las celdas fotoelectroquímicas, se analizan también otros parámetros tales como la densidad de corriente (mA/cm2), la tensión externa aplicada (V), el ratio de producción (mmol/l.h.cm2), la estabilidad (h) y la eficiencia, más conocida por su término en inglés «solar to fuel” (STF, %) [1].

Halmann et al. [3] reportaron en 1978 el primer estudio de una celda basada en un fotocátodo tipo p de fosfuro de galio que obtuvo metanol, formaldehído y ácido fórmico. Desde entonces hasta hoy, los grupos de investigación han focalizado sus estudios en las distintas configuraciones de las celdas fotoelectroquímicas y fotocatalíticas, así como en los materiales con los que construir los fotoelectrodos. Dependiendo de los materiales escogidos en los electrodos, del electrolito y de la energía aportada se puede obtener un producto u otro.
Durante mi estancia en el centro RCCS de la universidad Heriot-Watt en Edimburgo, he analizado sistemas fotoelectroquímicos (PEC) de producción de metano y sus eficiencias, así como sus similitudes y potenciales sinergias con otras tecnologías electroquímicas de conversión del CO2 en las que estoy desarrollando mi tesis doctoral en la universidad de León.
El desarrollo de esta tecnología de reducción solar directa de CO2 se encuentra a un nivel tecnológico bajo, a escala laboratorio (véase Figura 3).La investigación se está centrando principalmente en el estudio de nuevos materiales para los fotoelectrodos que sean más eficientes y abundantes en la naturaleza. Esta última condición es indispensable si se quiere desarrollar estas tecnologías bajo las premisas de sostenibilidad económica y medioambiental y, por qué no, de la geoestrategia.
* * *
Por Ruth Diego García, Ingeniera Industrial del Centro de Desarrollo Tecnológico de CIUDEN, y doctoranda en la Universidad de León.
***
Gracias al programa de movilidad CERU “On the move” y de la beca recibida por mi universidad (University de León, Department of Ingeniería Química Ambiental y Bioprocesos), realicé a finales de 2019 una estancia de investigación en el grupo RCCS, liderado por la profesora Mercedes Maroto-Valer, de la Universidad Heriot-Watt en Edimburgo. El RCSS trabaja en diferentes líneas de investigación sobre sistemas de captura, usos y almacenamiento del CO2 (CCUS, en sus siglas inglesas).
***
Más información: