Bienvenidos a la misión EXOSOMA XIII. Una vez encapsulados en membranas lipídicas de seguridad, acomodaos para descubrir las entrañas del tejido cardíaco en la galaxia Humana y preparaos para encontrar nuevas señales que ayuden a detectar fallos en el sistema cardiaco.
Nos encontramos en la gran estación cardíaca central. Como cada día, el caos y ajetreo de viajeras por la galaxia Humana es constante. Estas viajeras se liberan desde todos los tipos de células de nuestro corazón en forma de esferas. Se caracterizan por una membrana lipídica exterior que engloba una porción de la célula de origen como equipaje identificativo. Os presento a nuestras viajeras: las vesículas extracelulares. Con este término se engloba a una gran familia de vesículas. En ella, se distinguen diferentes tipos de estas viajeras en función de su origen, su tamaño, su equipaje y su mecanismo de partida. Sin embargo, debido a que son los pequeños de la familia, junto a su reciente auge en diversas anomalías de la galaxia Humana, nuestros viajeros estrella son los exosomas. Su misión es viajar de unas células a otras, actuando como mensajeros esenciales de la comunicación celular. Su equipaje conforma el mensaje que van a transmitir a la célula de destino, el cual está determinado por el tipo celular y las condiciones de las que parten. Además, una parte de esta carga es común a la mayoría de ellos, gracias a la cual los podemos distinguir entre el resto de viajeras.
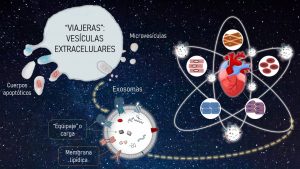
Hoy es un día especialmente agitado, las alarmas de descenso de nivel de glucosa y oxígeno en el puesto de control han saltado: “¡Exosomas procedentes de músculo cardíaco con destino arteria coronaria, deben partir de inmediato! Por favor, no olviden su equipaje y protejan sus proteínas y ácidos nucleicos personales”.
Estos exosomas actúan como satélites diagnósticos del daño padecido. Gracias a ellos, podemos tener pistas que nos lleven a detectar posibles fallos cardiacos, como en este caso, la falta de oxígeno y glucosa. Por ello, obtenerlos durante su viaje por las vías arteriales y venosas de la galaxia Humana, separarlos del resto de pasajeros e identificar su carga específica del fallo producido, constituye la misión EXOSOMA XIII.
Conocidas las bases de nuestra misión, aterrizamos con paso firme en el laboratorio. Dejamos a un lado este escenario novelesco y cambiamos la escafandra por la bata y los guantes, para extraer de entre tanta aparente ficción nuestro verdadero trabajo.
Si algo ha quedado claro de esta simulación es que nuestro trabajo se centra en los exosomas. En concreto, el estudio de aquellos secretados por células del músculo cardiaco (cardiomiocitos) ante la falta de oxígeno y nutrientes, lo que denominamos una condición de isquemia. Como consecuencia de este fenómeno, ocasionado por una obstrucción arterial, se produce la lesión e incluso muerte de las células musculares. Este fenómeno se conoce clínicamente como síndrome coronario agudo (SCA), cuya manifestación clínica de mayor gravedad es, desafortunadamente mucho más popular: el infarto agudo de miocardio. Una de las respuestas de las células ante esta situación de daño, es la liberación al torrente sanguíneo de moléculas específicas, en mayor concentración que en condiciones normales. Por ese motivo, son empleadas como moléculas marcadoras de infarto, junto a otras herramientas diagnósticas estandarizadas. El problema de esta metodología radica en que los casos menos severos pueden pasar desapercibidos. Estos pacientes manifiestan síntomas clínicos ambiguos, no específicos de infarto, que dificultan su diagnóstico (1).
Por esta razón, nuestro objetivo es la búsqueda de nuevas moléculas marcadoras que, junto a las técnicas diagnósticas ya establecidas, ayuden en la identificación de pacientes de SCA sin una sintomatología evidente. En este punto entran en juego los exosomas. Las moléculas marcadoras de la falta de oxígeno y nutrientes, además de ser liberadas directamente a la sangre, pueden secretarse dentro de exosomas. Y como se ha descrito anteriormente, gracias a la dependencia de su carga con las condiciones y el origen celular, los exosomas se sitúan como potenciales herramientas diagnósticas en SCA (2).
Ahora bien, para poder alcanzar este objetivo, el trabajo de laboratorio parte de modelos más sencillos. En ellos, tratamos de reproducir el escenario dado en un paciente de SCA, que denominamos in vivo, mediante modelos celulares o también llamados in vitro.
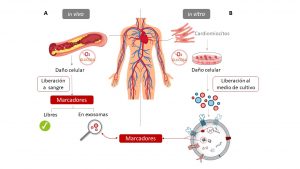
En primer lugar, establecemos un modelo celular de cardiomiocitos, es decir, cultivamos las células musculares del corazón que van a secretar los exosomas de interés. A continuación, imitamos las condiciones de isquemia dadas en un paciente de SCA. Para ello, suprimimos el aporte de glucosa y oxígeno. Ante este daño celular, los cardiomiocitos van a secretar exosomas al medio de cultivo, entre muchas otras partículas. Luego para poder estudiar la carga de los exosomas liberados, primero debemos aislar y purificar los exosomas del resto de “viajeras”: vesículas, moléculas del medio y restos en suspensión. Y en segundo lugar, nos aseguramos de que hemos separado mayoritariamente los exosomas y no hemos capturado muchas de las otras partículas. Para ello, comprobamos si el tamaño, la forma y el marcaje (esa parte de la carga común a la mayoría de exosomas) se corresponde con las características de los exosomas.
En este punto, por fin llegamos al momento más fascinante de la misión: ya podemos estudiar su contenido y por tanto, buscar a nuestras moléculas marcadoras. En concreto, nos centramos en el estudio de proteínas y de ácidos ribonucleicos de pequeño tamaño. Aquellas moléculas que identifiquemos en mayor abundancia en exosomas obtenidos bajo estas condiciones de isquemia simulada, podrían actuar como marcadores de SCA. Por consiguiente, una vez validadas, se podrían extrapolar a la búsqueda en exosomas obtenidos directamente de muestras de sangre de pacientes (escenario real), facilitando así su diagnóstico.
En definitiva, más allá de trabajar entre simulaciones, los resultados obtenidos de los modelos celulares que establecemos in vitro son el punto de partida para posteriores estudios in vivo. Gracias a estas aproximaciones, conseguimos identificar moléculas marcadoras de isquemia en el equipaje de los exosomas, debido a que son satélites diagnósticos de síndrome coronario agudo en la galaxia Humana. Con todo ello, nuestra misión EXOSOMA XIII quedaría finalizada con éxito.
Por Paula Gómara Utrilla (@PaulaGU_24), investigadora en el Grupo de Investigación de Progenitores Adultos del Sistema Cardiovascular, Instituto Aragonés de Ciencias de la Salud.
Más información:
- Hamm CW et al. (2011).
- Sluijter et al. (2014).
- Imágenes usadas en Figura 1:
- Galaxia: obtenida de Pxhere.
- Célula con tipos de vesículas extracelulares: adaptada de Sluijter et al. (2014).
- Exosomas: adaptada de Kalluri and LeBleu (2020).
- Corazón: obtenida de Freepik.
- Tipos celulares del tejido cardiaco: esquema adaptado de Jung JH et al. (2017).
- Images used in Figure 2:
- Sistema circulatorio: obtenida de Freepik.
- Arteria: obtenida de Freepik.
- Cardiomiocitos: adaptada de Lebeau et al. 2020.
- Placa de cultivo: obtenida de pngwing.
- Exosomas: adaptada de Kalluri and LeBleu (2020).